天演药业(以下简称“公司”或“天演”)(纳斯达克股票代码:ADAG)是一家平台驱动的临床阶段生物制药公司,致力于发现并开发以原创抗体为基石的新型癌症免疫疗法。公司今日发布,美国食品药品监视管理局(FDA)已同意其抗 CTLA-4单克隆抗体(mAb)ADG116 与抗PD-1 帕博利珠单抗结合疗法的Ib/II 期临床实验申请。该全球实验(ADG116-P001 / KEYNOTE-C97)将于美国及亚太地域(APAC)多个临床中心对晚期/转移性实体瘤患者进行评估。
ADG116凭借天演原创的新表位抗体 NEObody™ 平台技术,靶向 CTLA-4 的奇特保守表位,通过高效肃清肿瘤微环境中的调节性T细胞(Treg)并柔性阻断CTLA-4配体联合而激活T细胞,旨在增长有效性的同时改善产品安全性,有望战胜现有的抗CTLA-4疗法存在的安全性问题。
“FDA同意此临床实验是我们天演抗 CTLA-4 疗法开发筹划中的一个主要里程碑,标记着我们对ADG116 与抗 PD-1疗法结合用药进行评估的主要进展。”天演药业结合创始人、首席执行官兼董事长罗培志博士表现,“凭借新表位抗体 NEObodyTM 技术,ADG116 有望战胜抗 CTLA-4 疗法现存的安全性问题,从而实现更好的临床获益。而对 ADG116 与帕博利珠单抗联用的摸索旨在施展CTLA-4/PD-1 的双重阻断作用,平衡安全性和有效性以释放该结合疗法作为癌症治疗基石的潜力。”
ADG116-P001实验预计于2022年初进行首例患者给药,旨在评估安全性和耐受性,肯定最大耐受剂量,并评估ADG116与帕博利珠单抗结合用药的初步疗效。
此外,正在进行的 ADG116-1003 临床实验筹划通过两组结合队列评估 ADG116 与特瑞普利单抗或与ADG106 在晚期/转移性实体瘤患者中的安全性和初步疗效。
关于天演药业
天演药业(纳斯达克股票代码:ADAG)是平台驱动并拥有自主平台产出的临床产品开发阶段的生物制药公司,公司致力于发现并开发以原创抗体为基石的新型癌症免疫疗法。借力于计算生物学与人工智能,凭借其全球开创的三体平台技术(新表位抗体NEObody™,安全抗体SAFEbody™及强力抗体POWERbody™),天演药业已树立起聚焦于新型肿瘤免疫疗法的奇特原创的抗体产品线,以解决尚未满足的临床需求。天演已和多个全球知名合作伙伴达成了战略合作关系,并以其多种原创前沿科技为合作伙伴的新药研发赋能。
安全港声明
本新闻稿包括前瞻性声明,包含关于 ADG116 临床前研讨的声明、ADG116临床前研讨成果的潜在影响,以及天演药业的推动和预期的临床开发、监管里程碑和天演药业管道候选产品的商业化。由于各种主要因素,包含但不限于天演药业证明其候选药物的安全性和有效性的才能,实际成果可能与前瞻性陈说中指出的成果存在重大差别;其候选药物的临床成果,可能不支撑进一步开发或监管同意;相干监管机构就天演药业候选药物的监管同意做出决议的内容和时光;如果获得同意,天演药业为其候选药物取得商业胜利的才能; 天演药业为其技术和药物获得和维持知识产权掩护的才能; 天演药业依赖第三方进行药物开发、制作和其他服务; 天演药业有限的经营历史以及天演药业获得额外运营资金以及完成其候选药物的开发和商业化的才能; 天演药业在其现有战略伙伴关系或合作之外签署额外合作协定的才能,以及 COVID-19 对天演药业的临床开发、商业和其他运营的影响,以及在“风险因素”部分更充足讨论的那些风险在 天演药业提交给美国证券交易委员会的文件中。所有前瞻性陈说均基于天演药业当前可获得的信息,天演药业不承担公开更新或修订任何前瞻性陈说的任务,无论是由于新信息、未来事件或其他原因,除非法律可能要求。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20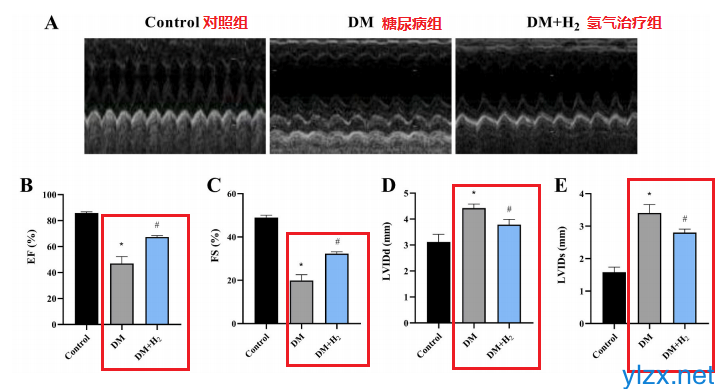
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20