聚焦于可突破血脑屏障的小分子靶向药物研发的生物医药创新企业ABM Therapeutics(璧辰医药)今日发布,其自主研发的BRAF克制剂ABM-1310临床实验申请获得中国国度药品监视管理局 (NMPA) 同意,批准公司针对BRAF突变的晚期实体瘤患者开展I期临床实验。这也是璧辰医药获得的中国首个IND批件。
ABM-1310是璧辰医药自主开发的创新小分子药物,具有优异的细胞膜渗透性。作为全球一款下一代入脑BRAF克制剂,目前临床I期实验正在美国顺利开展,初期数据已展示出良好的安全性和积极的信息。即将开启的中国临床I期,是一项开放式、多中心、剂量递增和扩大的研讨,旨在摸索ABM-1310在BRAF V600突变晚期实体瘤受试者中的安全性、耐受性、药代动力学以及初步抗肿瘤活性,为1b/2期临床研讨肯定最佳剂量。
对于在中国获得的首个IND批件,璧辰医药的创始人、董事长陈晨博士表现:“首先感激团队的尽力和他们的高效执行力。此次获批,是对团队自主研发才能的再一次认可,是公司发展史上又一个里程碑。很多晚期实体瘤病人死于脑转移这已经是不争的事实,但是目前的治疗方式还非常有限,患者的生存状态仍不容乐观,晚期实体瘤仍存在高度未被满足的临床需求。ABM-1310是一种新型小分子BRAF克制剂,具有很高的水溶性、细胞和血脑屏障通透性, 有望成为各种原发性脑瘤以及恶性肿瘤脑转移的新一代BRAF克制剂。我们将积极推动在中国的临床研讨,愿望早日造福病人。”
作为专注于可突破血脑屏障的新药研发领军企业,璧辰医药拥有丰硕的药物研发管线,已经成为极具特点的抗脑癌药物和其他入脑小分子药物的开发平台。公司将进一步开展同医院、制药企业的普遍合作,积极摸索有效的治疗方案,迅速推动临床研讨,为患者提供更多更有效的治疗选择。
关于璧辰医药
璧辰医药成立于2015年,是一家聚焦于可突破血脑屏障的小分子药物研发的生物医药创新企业,拥有胜利研发中枢神经体系和癌症全球新药的技术团队,以及高效的商务和公司营运团队。公司拥有丰硕的小分子入脑药物研发管线,拥有全球领先的BPKdd™入脑激酶新药研发平台,其自主研发的首款下一代入脑BRAF克制剂ABM-1310可以突破血脑屏障,使药物入脑效力明显进步,有望解决脑胶质瘤等原发性脑瘤,以及黑色素瘤、肺癌等多种肿瘤脑转移问题,其特征也合适于肿瘤微环境庞杂的结直肠癌。作为公司自主研发的第一个候选药物ABM-1310,于2019年11月29日获得FDA临床实验许可,目前已经在美国进行临床I期实验。美国临床实验登记号为:NCT04190628。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20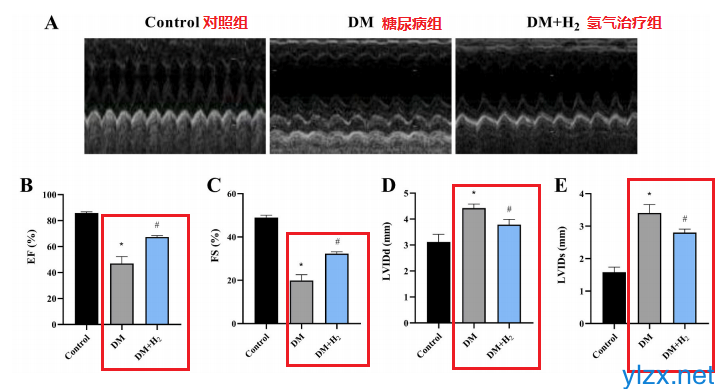
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20