驯鹿医疗,一家处于临床阶段、致力于细胞治疗和抗体药物开发和产业化的创新生物制药公司,今日与信达生物制药(简称“信达生物”)(香港联交所股票代码:01801),一家致力于研发、生产和出售用于治疗肿瘤、代谢疾病、自身免疫等重大疾病的创新药物的生物制药公司,共同发布美国食品药品监视管理局(FDA)孤儿药开发办公室(Office of Orphan Products Development, OOPD)已正式书面回函,授予两家公司共同开发的全人源自体B细胞成熟抗原(BMCA)嵌合抗原受体自体T细胞(CAR-T)注射液(驯鹿医疗研发代号CT103A,信达生物研发代号IB1326)孤儿药资历认定(Orphan Drug Designation, ODD),用于治疗复发/难治性多发性骨髓瘤(R/R MM)。
FDA孤儿药资历的认定可赞助加速药品在美国的临床开发和注册进度。CT103A候选产品将有资历享受若干优惠政策,包含FDA对临床研讨指点支撑、特别费用减免,以及同意上市后产品在美国的七年市场独占权等。2021年2月,CT103A用于R/R MM的疗法已被中国国度药品监视管理局(NMPA)药品审评中心(CDE)纳入“突破性治疗药物”品种。
驯鹿医疗首席执行官兼首席医学官汪文博士表现:
“FDA授予CT103A‘孤儿药’认定,对多发性骨髓瘤患者具有主要意义,代表着FDA对于CT103A候选产品的确定和驯鹿医疗提供的既往临床数据的认可。当前,驯鹿团队正在将CT103A的临床开发向前线治疗、结合用药、自身免疫性疾病适应症拓展、海外布局四个维度推动,期待这款候选产品早日上市,抢救更多患者的性命!”
信达生物高等副总裁兼周辉博士表现:
“FDA对IBI326的孤儿药认证是我们致力于开发有效性更优和存续性更强的BCMA靶向 CAR-T的一个里程碑,凸显了将这一治疗选择带给多发性骨髓瘤患者的主要性,也激励我们进一步加快IBI326的临床开发。愿望这款候选产品早日上市,给多发性骨髓瘤的患者带去愿望。”
关于FDA孤儿药资历认定
孤儿药认定(Orphan Drug Designation, ODD)是FDA 孤儿药产品开发办公室(Office of Orphan Products Development,OOPD)对符合条件的用于预防、治疗及诊断罕见病的药物(包含生物制品)授予的一种资历认定。孤儿药又称为罕见病药,指用于预防、治疗、诊断罕见病的药品,FDA针对罕见病有明白的界定尺度,即影响美国人群少于20万的疾病。由于罕见病患病人群少、市场需求少、研发成本高,很少有制药企业关注其治疗药物的研发,因此这些药被称为“孤儿药”。1983年美国公布《孤儿药法案》(Orphan Drug Act, ODA),规定凡获得孤儿药资历的候选药物,有机遇获得一系列配套支撑政策。
关于多发性骨髓瘤(MM)
多发性骨髓瘤(MM)是最常见的血液癌症之一,是一种克隆性浆细胞异常增殖的恶性疾病。对于初治的多发性骨髓瘤患者,常用的一线治疗药物包含蛋白酶体克制剂、免疫调节类药物及烷化剂类药物。对于大多数的患者,常用的一线治疗可以使患者的病情稳固3-5年,但也有少部分患者在初治时表示为原发耐药,病情不能得到有效掌握。对于治疗有效的大多数初治患者,在经过疾病稳固期后也会不可避免的进入复发、难治阶段。因此,复发/难治多发性骨髓瘤患者仍存在未满足的需求。在美国,MM约占所有新发癌症患者人数近2%,占癌症死亡患者人数的2%以上。
依据弗若斯沙利文报告:
美国MM的新发病人数从2016年30,300 人增长至2020年32,300人,预计2025年将增长至37,800人。美国MM的患病人数从2016年132,200人增长到2020年144,900人,预计2025年将增长至162,300人。
中国MM的新发病人数由2016年18,900人增至 2020年21,100人,预计2025年将增加至24,500人。中国MM的患病率从2016年69,800 人增至2020年113,800人,预计2025年增加至182,200人。
关于CT103A (BCMA CAR-T)
CT103A是由驯鹿医疗和信达生物制药结合开发的一种创新候选产品。本候选产品以慢病毒为基因载体转染自体T细胞,CAR包括全人源scFv、CD8a 铰链和跨膜、4-1BB共刺激和CD3ζ激活构造域。基于严厉的筛选,通过全面的体内外功能评价,CT103A CAR-T候选产品具有强有力和迅速的疗效,并有突出的持久性。2021年2月,CT103A获国度药监局“突破性治疗药物”认定,用于治疗复发难治性多发性骨髓瘤。2022年2月, CT103A获美国食品药品监视管理局“孤儿药”认定,用于治疗复发难治性多发性骨髓瘤。
关于驯鹿医疗
驯鹿医疗是一家专注于细胞治疗和抗体药物开发和产业化的创新生物制药公司。公司以开发血液肿瘤细胞类药物和抗体药物为创新的基石,向实体瘤和自身免疫疾病拓展,拥有完全的从早期发现、注册申报、临床开发到商业化生产的全流程平台才能及包含了全人源抗体发现平台、高通量CAR-T药物优选平台、通用CAR技术平台、生产技术平台、临床转化研讨平台在内的多个技术平台。现有10个在研品种处于不同研发阶段,其中进展最为快速的候选产品CT103A(全人源BCMA嵌合抗原受体自体T细胞注射液)已处于临床开发后期阶段,已于2021年2月被国度药品监视管理局(NMPA)药品审评中心(CDE)纳入“突破性治疗药物”品种;公司自主研发的创新候选产品CT120(全人源CD19/CD22双靶点CAR-T细胞注射液)已进入临床研讨阶段,并已获得FDA孤儿药认定(ODD)。
凭借强执行力的管理团队、丰硕的产品管线、奇特的创新研发与商业模式,驯鹿医疗有志于成为业界有影响力的创新药企,将真正解决临床痛点、具有市场竞争力的创新药物推向临床直至市场,为受试者开拓新的治疗途径,带来新的愿望。
关于信达生物
“始于信,达于行”,开发出老百姓用得起的高质量生物药,是信达生物的幻想和目的。信达生物成立于2011年,致力于开发、生产和出售用于治疗肿瘤、自身免疫、代谢疾病等重大疾病的创新药物。2018年10月31日,信达生物制药在香港结合交易所有限公司主板上市,股票代码:01801。
自成立以来,公司凭借创新结果和国际化的运营模式在众多生物制药公司中脱颖而出。树立起了一条包含29个新药品种的产品链,笼罩肿瘤、代谢疾病、自身免疫等多个疾病范畴,其中6个品种入选国度“重大新药创制”专项。公司已有6个产品(信迪利单抗注射液,商品名:达伯舒®,英文商标:TYVYT®;贝伐珠单抗生物相似药,商品名:达攸同®,英文商标:BYVASDA®;阿达木单抗生物相似药,商品名:苏立信®,英文商标:SULINNO®;利妥昔单抗生物相似药,商品名:达伯华®,英文商标:HALPRYZA®;pemigatinib口服克制剂,商品名:达伯坦®,英文商标:PEMAZYRE®;奥雷巴替尼片,商品名:耐立克®)获得同意上市,5个品种进入III期或要害性临床研讨,另外还有18个产品已进入临床研讨。
信达生物已组建了一支具有国际先进程度的高端生物药开发、产业化人才团队,包含众多海归专家,并与美国礼来制药、Adimab、Incyte、MD Anderson 癌症中心和韩国Hanmi等国际合作方达成战略合作。信达生物愿望和大家一起尽力,进步中国生物制药产业的发展程度,以满足百姓用药可及性和人民对性命健康美妙希望的寻求。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20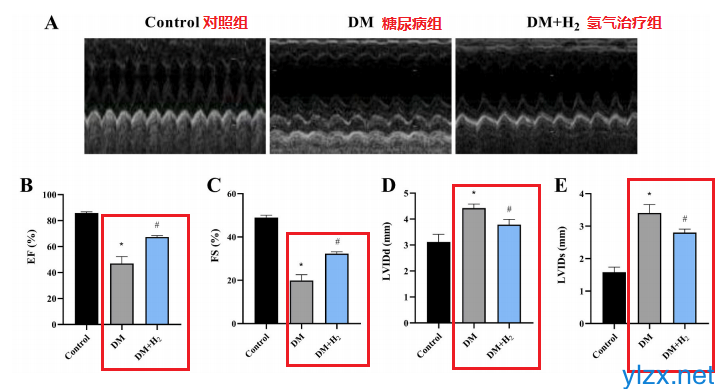
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20