拥有首创性细胞外囊泡(EV)平台技术的再生生物技术公司Direct Biologics今天发布,FDA已同意该公司进行一项3期实验,使用其实验性EV药物ExoFlo治疗新冠肺炎引起的急性呼吸窘迫综合征(ARDS)。Direct Biologics是第一家也是迄今为止唯一一家获得FDA的3期临床实验新药(IND)适应症同意的EV公司。
此项3期临床实验将在FDA同意的首个EV治疗药物再生医学先进疗法(RMAT)项目标支撑下进行,这使得Direct Biologics成为FDA历史上仅有的70家正式获得RMAT的公司之一。与迅速通道和突破性疗法认定一样,FDA创建的RMAT针对证明能治疗危及性命的严重疾病的有远景的再生药物,旨在加快其审批进程。
结合创始人兼首席执行官Mark Adams表现:"获得FDA关于3期实验的同意是Direct Biologics的一个要害里程碑。这一同意再加上RMAT认定,让我们能够加速实现这种有可能拯救性命的药物ExoFlo的商业化。 这项名为‘根除新冠肺炎'的3期实验是一项国际性、多中心、双盲、随机、抚慰剂对比的3期实验。 我们的目的是在美国、西班牙、印度、约旦、埃及、黎巴嫩和南非的医院地点招募ARDS患者,并证明与仅使用尺度护理相比,使用ExoFlo治疗后的死亡率明显降低。 作为再生医学治疗范畴的先驱,Direct Biologics正在转变医学的未来。"
结合创始人兼总裁Joe Schmidt表现:"不管新冠肺炎仍是全球性流行病还是已经成为一种处所性流行病,有一个范畴的需求始终未得到满足:针对ARDS的有效治疗方式。 65岁以上及有合并症的人群一旦沾染SARS-CoV-2病毒,都将很容易发展为严重沾染和ARDS。我们的2期临床实验显示,ExoFlo具有壮大的安全性,并有望降低60天死亡率,表明ExoFlo可以对ARDS住院患者起到抢救性命的重大作用。获得FDA同意进行3期实验是一项宏大的成绩,因为目前还没有已知的ARDS治疗方式。 世界各地的医生和患者长期以来一直在等候解决方案。"
首席医疗官Vik Sengupta表现: "参与ExoFlo的开发是一项荣誉,越来越多的临床数据表明,ExoFlo是一种给治疗这种疾病带来愿望的药物,这种疾病的尺度治疗方式几十年来都没有取得任何改良。这种愿望在接受ExoFlo治疗的患者的阅历中得到了最深入的体现。就在上周,弗吉尼亚州一名妇女因新冠肺炎诱发的ARDS而使用呼吸机已达2个月,身材衰弱的她与其子女做最后的团聚。但作为抢救患者性命的最后一次尝试,重症监护室的医生恳求用ExoFlo作为同情用药对她进行治疗,而她奇迹般地康复了。而数百万像她这样的患者永远都未能康复出院。我们愿望将ExoFlo确立为ARDS的黄金治疗尺度,让世界各地医院的患者都能得到这种药物的治疗,从而转变这一局势。"
关于Direct Biologics
Direct Biologics的总部位于德克萨斯州奥斯汀,是一家市场领先的再生医学产品创新企业和cGMP制作商。 其旗舰产品ExoFlo包括调节蛋白、microRNA和负责细胞间通讯的信使RNA情势的数千种信号。 ExoFlo应用间充质干细胞(MSC)的自然治愈才能,无需添加干细胞本身。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20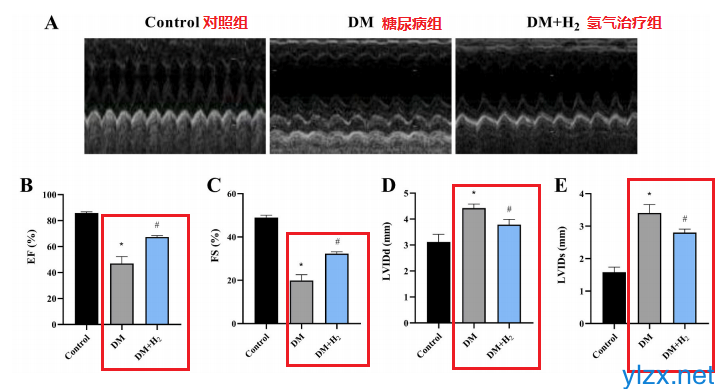
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20