5月 9 日,新加坡领先创新生物药公司 -- SCG(星汉德生物)发布,公司产品SCG101 -- 用于治疗HBV相干肝细胞癌的新型TCR-T细胞治疗产品,已经获得新加坡药监局(HSA)的IND同意。而就在3月初,SCG101刚刚获得中国药品监视管理局(NMPA)的IND同意,成为NMPA同意的首个用于治疗肝癌的TCR-T细胞治疗产品。
新加坡国度大学癌症研讨所Yong Wei Peng医生表现:"肝癌是癌症相干死亡最常见的原因之一,现有治疗方案在满足患者需求方面存在重大挑战,SCG101的IND获批将有望为亚太地域甚至全球的肝癌患者提供一种新的治疗方案"。
新加坡国度癌症中心首席研讨员Toh Han Chong教授表现:"细胞疗法是治疗癌症等要挟性命的疾病最有前程和发展最快的疗法之一, SCG101细胞治疗作为最领先的个体化癌症治疗方案,为新加坡的肝癌患者带来了新的愿望"。
SCG首席执行官王建立表现,全球规模内肝癌是死亡率第二高的癌症,每年导致超过70万人死亡。而从病例散布来看,全球每五个新增肝癌病例中就有四个在亚太地域,中国则更是占了一半。新加坡作为东南亚的医疗中心,也是世界顶级医疗旅游目标地,本次中国和新加坡的IND双获批,未来可以满足亚太地域肝癌患者需求, 符合公司预期,也是公司细胞治疗全球布局的既定部分。
对于SCG来说,此次在新加坡获得IND审批也属意料之中。依据新加坡药监局(HSA)官网显示,早在2021年HSA就发布SCG成为其官方合作伙伴,并共同评估和验证了SCG细胞治疗的制作工艺,该验证成果完整支撑公司自主研发产品SCG101 TCR-T细胞治疗IND申请,印证了SCG在新加坡的受器重水平和细胞治疗的领先位置。
众所周知,新加坡很早就将生物医药产业纳入国度层面战略规划,从2000年到2019年,新加坡的生物医药制作业复合年增加率达9%。全球前十且收益最高的跨国医药巨头GSK、诺华、罗氏、赛诺菲和默沙东等均已把亚太地域总部、大型制作工厂或研发中心设在了新加坡。而SCG从成立之初,就具备了国际化的"基因",公司全球总部设立在新加坡,在德国、新加坡和中国设有研发、转化和临床中心,同步IND全球化布局成为SCG的核心竞争优势,必将助力SCG向成为亚太领先生物药企途径上更进一步。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20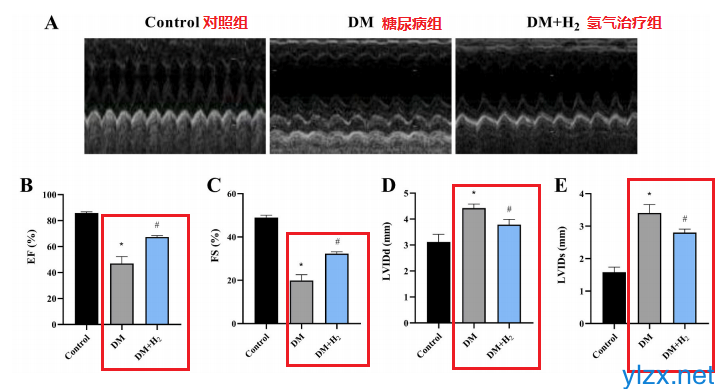
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20