据国度药监局官网资讯,为进一步增强药品监视管理,国度药监局近日宣布《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》(以下简称《征求意见稿》),向社会公开征求意见。意见反馈截止时光为2022年6月9日。
其中,《征求意见稿》提出,国度勉励儿童用药品和罕见病药品的的研制和创新,勉励仿造药发展。对首个同意上市的儿童专用新品种、剂型和规格,同意上市的罕见病新药,首个挑战专利胜利并首个获批上市的化学仿造药,给予必定的市场独占期。
勉励创新
加快上市通道
据悉,《征求意见稿》包含总则、药品研制与注册、药品上市许可持有人、药品生产、药品经营、医疗机构药事管理、药品供给保障、监视管理、法律责任、附则共十章181条,与现行《中华人民共和国药品管理法实施条例》共十章80条相比,增长了101条。
在药品研制与注册方面,《征求意见稿》提出勉励创新。国度完美药物创新系统,支撑药品的基本研讨、利用研讨和原始创新,支撑以临床价值为导向的药物创新,支撑企业采取先进技术设备进步药品安全程度,在科技立项、融资、信贷、招标采购、支付价钱、医疗保险等方面予以支撑。
国度支撑中药传承和创新,树立合适中药特色的审评审批系统,勉励运用现代科学技术和传统中药研讨方式开展中药的科学技术研讨和药物开发。增进中药现代化、国际化。
另外,《征求意见稿》提出,国务院药品监视管理部门树立突破性治疗药物、附条件同意上市、优先审评审批及特殊审批制度,勉励药物研发创新,缩短药物研发和审评过程。
勉励儿童用药品研制和创新
在儿童用药方面,《征求意见稿》提出,国度勉励儿童用药品的研制和创新,支撑药品上市许可持有人开发符合儿童生理特性的儿童用药品新品种、新剂型、新规格,对儿童用药品予以优先审评审批。在药物研制和注册申报期间,增强与申办者沟通交换,增进儿童用药品加快上市,满足儿童患者临床用药需求。
对首个同意上市的儿童专用新品种、剂型和规格,以及增长儿童适应症或者用法用量的,给予最长不超过12个月的市场独占期,期间内不再同意雷同品种上市。
对罕见病新药给予最长不超过7年的市场独占期
罕见病方面,《征求意见稿》提出,国度勉励罕见病药品的研制和创新,支撑药品上市许可持有人开展罕见病药品研制,勉励开展已上市药品针对罕见病的新适应症开发,对临床急需的罕见病药品予以优先审评审批。在药物研制和注册申报期间,增强与申办者沟通交换,增进罕见病用药加快上市,满足罕见病患者临床用药需求。
对同意上市的罕见病新药,在药品上市许可持有人许诺保障药品供给情形下,给予最长不超过7年的市场独占期,期间不再同意雷同品种上市。药品上市许可持有人不实行供给保障许诺的,终止市场独占期。
勉励仿造药发展
《征求意见稿》还提出, 国度勉励仿造药发展,对首个挑战专利胜利并首个获批上市的化学仿造药,给予市场独占期。
国务院药品监视管理部门在该药品获批之日起12个月内不再同意同品种仿造药上市,共同挑战专利胜利的除外。市场独占期限不超过被挑战药品的原专利权期限。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20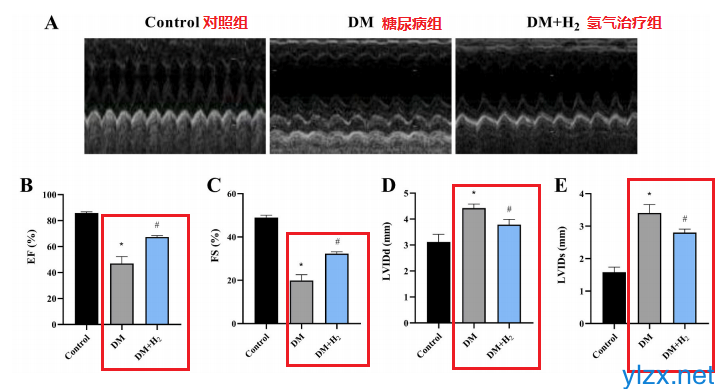
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20