和黄医药(中国)有限公司(简称“和黄医药”或“HUTCHMED”)(纳斯达克/伦敦证交所:HCM;香港交易所:13)今日发布, 达唯珂®(TAZVERIK®,通用名:他泽司他/ tazemetostat)的临床急需进口药品申请获海南省卫生健康委员会和海南省药品监视管理局同意,于海南博鳌乐城国际医疗旅游先行区(简称“海南先行区”)使用,用于治疗某些上皮样肉瘤和滤泡性淋巴瘤患者,与美国食品药品监视管理局(“FDA”)已同意的标签一致。国务院于2013年同意设立海南先行区,汇聚全球科技创新并成为国际医疗旅游目标地。2020年,海南先行区招待医疗旅客达8.39万人次。
达唯珂®是由Epizyme, Inc.(“Epizyme”)开发的EZH2[1]甲基转移酶克制剂,已分离于2020年1月和2020年6月获FDA同意用于治疗某些上皮样肉瘤患者和某些滤泡性淋巴瘤的患者。
和黄医药首席执行官兼首席科学官苏慰国博士表现:“此次达唯珂®在海南先行区获批,令患者得以及早获得这种全球开创的EZH2克制剂。和黄医药致力为有须要的患者带来创新药物。除了海南先行区以外,依据我们和Epizyme的合作协定,我们亦筹划在中国开展进一步的注册性研讨,赞助更多患者获得更便捷的治疗。”
2021年8月,和黄医药与Epizyme开展合作,在中国大陆、香港、澳门和台湾进行达唯珂®的研讨、开发、生产以及商业化。
关于滤泡性淋巴瘤和上皮样肉瘤
滤泡性淋巴瘤(FL)是非霍奇金淋巴瘤的一种亚型。滤泡性淋巴瘤约占非霍奇金淋巴瘤的17%。2020年,中国和美国估量分离新增16,000例和13,000例滤泡性淋巴瘤患者。[2],[3],[4]
上皮样肉瘤(ES)是一种罕见的、生长迟缓的软组织癌。根治性肿瘤切除术是上皮样肉瘤患者的重要治疗方式。然而,上皮样肉瘤容易产生局部复发和远处转移。由于治疗选择非常有限,上皮样肉瘤患者的存活率一般并不幻想。[5]
关于达唯珂®(TAZVERIK®,通用名:他泽司他/ tazemetostat)
达唯珂®是甲基转移酶克制剂,在美国获批用于治疗以下患者:
患有不符合完整切除条件的转移性或局部晚期上皮样肉瘤的成人及16岁及以上的儿童患者。
复发或难治性滤泡性淋巴瘤的成人患者,其肿瘤经FDA同意的实验检测呈EZH2突变阳性,并且之前已经接受至少两种全身治疗。
复发或难治性滤泡性淋巴瘤的成人患者,惟并无任何幻想的替代治疗方案。
上述适应症依据客观缓解率(ORR)及和缓解连续时光(DOR)获美国FDA加速审批后获得同意。依据这些适应症继续授予的同意可能取决于确证性实验中的临床疗效验证和描写。
关于他泽司他在中国的其他临床开发筹划
和黄医药及Epizyme正在大中华区开发他泽司他用于治疗多种血液肿瘤及实体瘤,其中和黄医药主导Epizyme的SYMPHONY-1研讨的中国部分。和黄医药还筹划与Epizyme合作开展其他全球研讨。
SYMPHONY-1研讨(原称EZH-302) 是一项全球、多中心、随机、双盲、活性对比、三阶段、生物标记物富集的确证性Ib/III期研讨,旨在评估他泽司他和R2方案结合疗法治疗既往接受过至少一线治疗后复发或难治性滤泡性淋巴瘤患者的安全性和疗效(clinicaltrials.gov 注册号:NCT04224493)。
我们筹划启动一项滤泡性淋巴瘤的桥接研讨,以支撑他泽司他在中国的注册,以及启动他泽司他与和黄医药其他药物的多项结合疗法研讨。
关于和黄医药
和黄医药(纳斯达克/伦敦证交所:HCM;香港交易所:13)是一家处于商业化阶段的创新型生物医药公司,致力于发现、全球开发和商业化治疗癌症和免疫性疾病的靶向药物和免疫疗法。团体旗下公司共有超过4,600名员工,其中核心的肿瘤/免疫业务拥有约1,700人的团队。自成立以来,和黄医药已将自主发现的12个候选癌症药物推动到在全球开展临床研讨,其中首三个创新肿瘤药物现已在中国获批上市。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20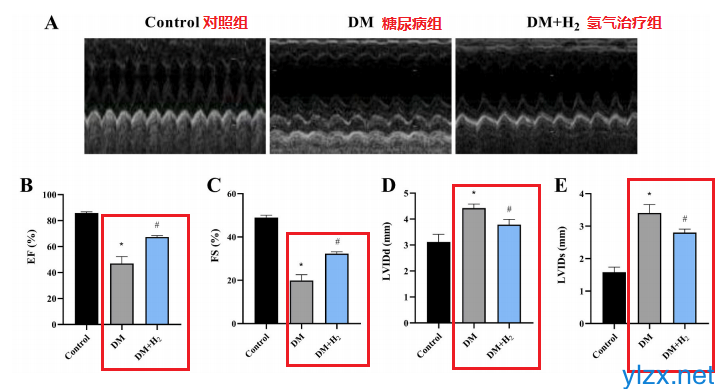
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20