歌礼制药有限公司(香港联交所代码:1672,简称“歌礼”)今日发布:歌礼药业(浙江)有限公司(简称“歌礼药业”)与中国医药保健品有限公司已签订经销商协定,中国医药保健品有限公司成为歌礼药业利托那韦片在中国大陆地域的经销商。歌礼药业是歌礼全资从属公司,中国医药保健品有限公司是中国医药健康产业股份有限公司(简称“中国医药”)的全资从属公司。
利托那韦片是多种针对病毒蛋白酶的口服抗病毒药物的药代动力学加强剂。歌礼拥有目前中国唯一通过生物等效性研讨获批上市的利托那韦口服片。歌礼利托那韦口服片于2021年9月获中国国度药品监视管理局同意上市(药品同意文号:国药准字H20213698)。
歌礼已向12个欧洲国度(德国、法国、爱尔兰、英国、西班牙、葡萄牙、意大利、比利时、波兰、瑞典、荷兰和丹麦)和中国香港递交了利托那韦(100毫克薄膜衣片)上市许可申请。
中国医药董事长、党委书记李亚东表现:“中国医药作为医药行业国度队,始终践行‘守护人民健康’初心使命,愿望以此为契机摸索与以歌礼为代表的中国创新药企业的多层面合作,共同助力实现‘健康中国2030’的雄伟目的。”
歌礼创始人、董事会主席兼首席执行官吴劲梓博士表现:“非常幸运与中国医药达成商业化合作。中国医药是国内领先的药品分销商,拥有笼罩全国的抗病毒药物出售终端网络。歌礼抗病毒管线已上市产品包含中国唯一通过生物等效性实验获批上市的利托那韦片。我们期待与中国医药携手合作,双方依托各自产品与资源优势,共同为打消传染性疾病尽企业的社会责任。”
歌礼已上市抗病毒产品还包含被纳入《国度基础医疗保险、工伤保险和生育保险药品目录(2021年)》的新力莱®(盐酸拉维达韦)结合戈诺卫®(达诺瑞韦钠)的全口服直接抗丙肝病毒方案。
歌礼在研抗病毒管线还包含乙肝功能性治愈、艾滋病功能性治愈等待选药物。
关于中国医药
中国医药是在上海证券交易所挂牌的国有控股上市公司(证券代码:600056),致力于医药产业发展和人类健康事业,尽力打造中国医药健康产业范畴的旗舰企业。近年来,公司初步树立了以国际贸易为引领、以医药工业为支持、以医药商业为纽带的贸、工、技、服一体化产业格式,产业形态涉及种植加工、研发、生产、出售、物流、进出口贸易、学术推广、技术服务等全产业链条。依据颁布的威望行业排名,公司位列 2020 年度中国医药工业百强榜化药企业排名第 35 位;中国医药-重庆医药结合体位列 2020 年医药流通百强第 5 位。
关于歌礼
歌礼是一家在香港证券交易所上市(1672.HK)的创新研发驱动型生物科技公司,涵盖了从新药发现和开发直到生产和商业化的完全价值链。歌礼致力于病毒性疾病、非酒精性脂肪性肝炎/原发性胆汁性胆管炎、肿瘤(口服肿瘤代谢检讨点与免疫检讨点克制剂)等范畴创新药的研发和商业化,以解决国内外患者临床需求。在具备深厚专业知识及优秀过往成绩的管理团队率领下,歌礼以全球化的视野布局创新药物研发范畴,瞄准未被满足的临床需求,并以研发赛道国际领先的定位,高效、迅速推动管线产品的开发。歌礼目前拥有三个商业化产品和20条强壮且聚焦创新的研发管线,众多在研管线处于国际领先的位置,并积极布局新的治疗范畴:
1. 病毒性疾病:(1)乙肝(功能性治愈):摸索以皮下注射PD-L1抗体ASC22及派罗欣®为基石药物,与其他靶点药物结合的治疗方案,有望为乙肝功能性治愈带来重大突破。(2)新冠肺炎药物管线:目前包含(i)已上市的利托那韦口服片剂(100 mg);(ii)口服聚合酶(RdRp)克制剂ASC10;(iii)口服蛋白酶(3CLpro)克制剂ASC11。(3)艾滋病:免疫疗法ASC22,用于艾滋病特异性免疫重建,以期实现艾滋病沾染者的功能性治愈。(4)丙肝:歌礼胜利研发上市由两个1类新药戈诺卫®和新力莱®组成的全口服丙肝治疗方案。
2. 非酒精性脂肪性肝炎/原发性胆汁性胆管炎:歌礼旗下全资子公司甘莱专注于非酒精性脂肪性肝炎范畴创新药的开发和商业化。甘莱有三款分离针对脂肪酸合成酶(FASN)、甲状腺激素ß受体(THRß)及法尼醇X受体(FXR)的处于临床阶段的非酒精性脂肪性肝炎候选药物及三种固定剂量复方制剂。针对FXR靶点的新药同时被开发用于原发性胆汁性胆管炎的治疗。
3. 肿瘤(口服肿瘤代谢检讨点与免疫检讨点克制剂):歌礼在肿瘤治疗范畴布局创新且具有差别化的管线,专注于在肿瘤脂质代谢中起要害作用的脂肪酸合成酶口服克制剂管线以及新一代免疫检讨点克制剂-口服PD-L1小分子克制剂管线。
4. 拓展性适应症:痤疮:ASC40继非酒精性脂肪性肝炎、实体瘤适应症后,新痤疮适应症已获批进入II期临床。

多样化、复合式流传,晋升本市医院和医
市健康增进委员会办公室、市卫生健康委组织上海市健康增进中心、复旦大学公共卫生学院在...(154)人阅读时间:2022-12-20
45个抗癌药品和19个罕见病药品参加第三批
为勉励制药产业发展,降低患者用药成本,2022年11月21日,财政部等部门结合宣布《关于宣...(198)人阅读时间:2022-12-20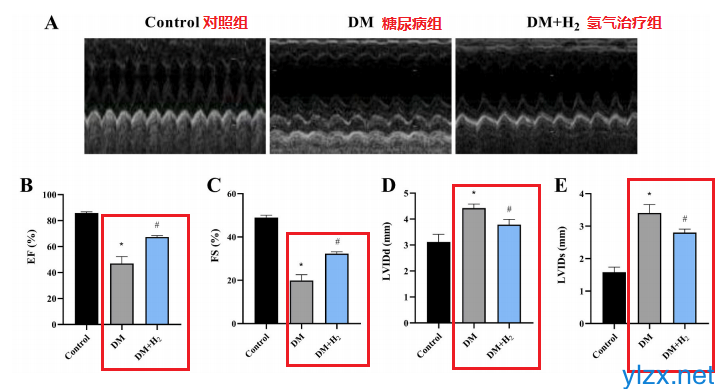
氢气结合药物对糖尿病及并发症(如糖尿
【背景介绍】糖尿病会引起多种并发症,在中老年人群中,糖尿病心脏病是糖尿病患者致死的...(241)人阅读时间:2022-12-20
第三批抗癌药品和罕见病药品可享增值税
记者21日从财政部了解到,为勉励制药产业发展,降低患者用药成本,财政部、海关总署、...(403)人阅读时间:2022-12-20
玛西普首次亮相CMEF,六大创新场景引领健
创新科技,智领未来,11月23日,第86届中国国际医疗器械博览会(CMEF)在深圳国际会展中心(宝安...(493)人阅读时间:2022-12-20